Для грибов
характерен окислительный тип метаболизма. Это не озна чает, что грибы не
способны к анаэробному расщеплению углеводов, т.е. не могут их сбраживать (ведь
спиртовое брожение осуществляется как раз дрожжами!); однако в анаэробных условиях
сколько-нибудь длительный рост грибов невозможен. Кроме того, основными продук
тами брожения оказываются этанол или молочная кислота. Другие ор ганические
кислоты образуются только в аэробных условиях.
В
естественных местах обитания грибов, т. е. в почве, никогда не бы вает
заметного накопления промежуточных продуктов их жизнедеятель ности. При
недостатке питательных веществ грибы получают максимум энергии и образуют
клеточные вещества за счет полного окисления и ассимиляции субстрата. Если в
лабораторных условиях и в промыш ленной практике дело обстоит иначе и
многочисленные продукты обме на выделяются в среду, то это следует объяснить
избыточным снабже нием грибов углеводами и известной «дезорганизацией» их
метаболиз ма, которой часто способствует исключение из среды некоторых
микроэлементов.
Известно, что
грибы обладают мощной гликолитической системой. В «узких местах» метаболических
путей происходит накопление проме жуточных продуктов, которые прямо или после
назначительных хими ческих изменений выделяются в среду. Дж. Фостер особо
подчеркивал отклонения в обмене веществ, возникающие при избытке субстрата. В
конечном счете большинство неполных окислений связано с наруше нием регуляции
метаболизма.
Во многих
случаях достаточно удалить какой-нибудь необходимый микроэлемент, чтобы
промежуточные продукты начали выделяться в среду. Значительное влияние
оказывает изменение концентрапии цин ка, железа, марганца, меди, а также
магния, калия и кальция (см. рис. 10.1). 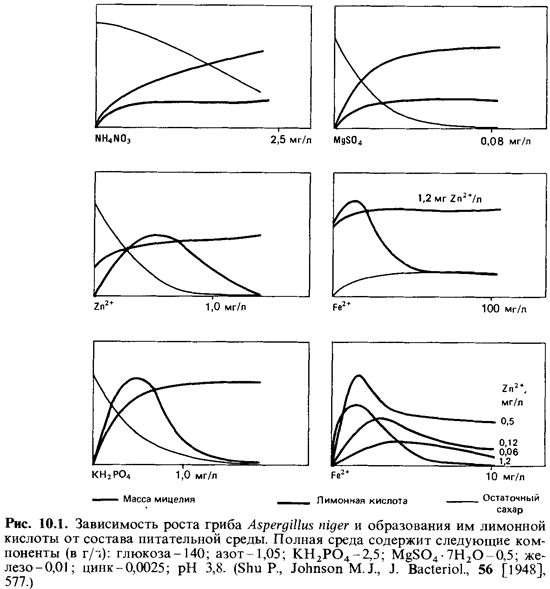
Молочную
кислоту выделяют главным образом представители по рядка Mucorales (Rhizopus nodosus, R.oryzae, R. arrhizus, R. nigricans) и
другие фикомицеты (Allomyces, Saprolegnia, Blastocladiella). Однако
у грибов она никогда не бывает единственным продуктом, как у
гомо-ферментативных молочнокислых бактерий. Наряду с молочной кисло той грибы
образуют в небольших количествах фумаровую, янтарную, яблочную, муравьиную и
уксусную кислоты, а также этанол. Для полу чения максимального выхода молочной
кислоты необходимо присут ствие 02. Поскольку грибы не нуждаются в
сложных питательных средах и в качестве источника азота довольствуются
мочевиной, получать молочную кислоту в особо чистом виде с помощью грибов
проще, чем использовать молочнокислое брожение, осуществляемое лактобацилла-ми.
Способность к
образованию фумаровой кислоты характерна для многих
родов Mucorales (Mucor, Cunninghamella, Circinella, Phizopus).
Глюконовую
кислоту образуют многие аспергиллы и пенициллы. Это продукт
ферментативного окисления глюкозы глюкозооксидазой, выделяемой
грибами в питательную среду. У Aspergillus niger этот про
цесс может идти с высоким выходом даже в 30-35%-ных растворах глюкозы, если
выделяющуюся кислоту нейтрализовать карбонатом кальция.
Глюкозооксидаза
представляет собой фермент, содержащий в каче стве простетической группы FAD.
При окислении глюкозы под дей ствием этого фермента как промежуточный продукт
образуется P-D-глюконо-5-лактон, который затем спонтанно или же с помощью
другого фермента-глюконолактоназы-присоединяет воду и превра щается в
глюконовую кислоту. Восстановленная глюкозооксидаза пере носит водород на
кислород воздуха с образованием перекиси водорода, которая затем под действием
каталазы может расщепляться на воду и кислород.
Щавелевую
кислоту выделяют многие грибы. Ее образованию спо собствует щелочная
реакция питательной среды.
Много работ
посвящено образованию лимонной кислоты, особенно техническим и
экономическим аспектам ее производства. После того как Вемер в 1893 году
обнаружил лимонную кислоту в культурах грибов (Citromyces pfefferianus), Кюрри
в 1917 году разработал основы полу чения ее в промышленном масштабе; он
установил, что Aspergillus niger превосходно растет на
средах с начальными значениями рН от 2,5 до 3,5 и выделяет при этом большие
количества лимонной кислоты. С по вышением рН появляется сначала глюконовая
кислота, а затем щавеле вая. Низкое начальное значение рН имеет то
преимущество, что позво ляет не опасаться бактериального загрязнения.
Промышленное
производство лимонной кислоты до сих пор часто ведется без соблюдения
стерильности, поверхностным способом в кюветах. В бро дильные камеры помещают
алюминиевые кюветы (размером 2 х 2,5 х 0,15 м), заполненные на высоту 8 см раствором мелассы, и
после инокуляции спорами гриба выдерживают их 9-11 дней при 30°С. Выход
продукта получается весьма значительным. После спуска питательной среды можно
снова подвести под ми целий гриба свежий раствор. Лимонную кислоту осаждают из
переработанного раствора, добавляя карбонат кальция, а затем
перекристаллизовывают и выде ляют с помощью серной кислоты. В настоящее время
при производстве лимон ной кислоты все более широко применяют глубинный метод.
Зависимость
образования лимонной кислоты от состава среды осо бенно четко выражена у Aspergillus niger.В
этом легко убедиться, изме няя содержание одного из компонентов среды при
сохранении всех про чих условий. Если к простой среде с глюкозой после удаления
микроэлементов (их осаждают гидроокисью алюминия) прибавлять определенные
компоненты в известных концентрациях, а затем иноку-лировать среду и после
9-дневной инкубации в колбах со встряхиванием определять массу мицелия,
остаточное количество сахара и количество образовавшейся лимонной кислоты, то
можно установить ряд инте ресных соотношений (рис. 10.1). Приведенные кривые
позволяют сде лать следующие выводы: а) нитрат аммония и сульфат магния не
оказывают какого-либо специфического влияния на выход лимонной кислоты-они
влияют только на рост мицелия; б) кривые для цинка, же леза и фосфора
характеризуются четким пиком. При концентрациях, обеспечивающих лишь
субоптимальный рост мицелия, отмечается бо лее высокий выход лимонной кислоты;
однако при дальнейшем сниже нии концентрации этих трех элементов торможение
роста мицелия ограничивает и выработку кислоты; в) особенно высокие выходы мож
но получить в тех случаях, когда два компонента - железо и цинк-при сутствуют в
лимитирующих количествах. Марганец оказывает отчетли вое подавляющее действие:
3 мкг Мп2 + на 1 л среды уже снижают выход
кислоты (между тем при использовании очищенной продажной глюкозы на каждый литр
среды вместе с 140 г
этого сахара вносится 10мкг Мп2+ !).
Повышенное
выделение лимонной кислоты при недостатке железа объясняется скорее всего тем,
что железо выступает в роли кофактора аконитазы, медь же действует по отношению
к нему как антагонист. На этом основан новый технический прием, повышающий
выход нужного продукта: даже в присутствии небольших количеств ионов железа в
рас творе мелассы (10 мг на 1 л)
можно получить максимальный выход ли монной кислоты, добавив к среде избыток
ионов меди (150 мг на 1 л).
Итаконовую
кислоту образуют лишь немногие штаммы Aspergillus itaconicus и A. terreus. Этот
процесс тоже происходит при рН среды около 2,0.
Химизм
образования кислот у грибов. Не подлежит сомнению, что в образовании
различных кислот из глюкозы участвуют реакции цикла трикарбоновых кислот
(«цикла лимонной кислоты»). Есть основания предполагать, что яблочная,
фумаровая, янтарная и лимонная кислоты образуются так, как это описано для
цикла трикарбоновых кислот, а за тем непосредственно выделяются в среду (рис.
10.2). 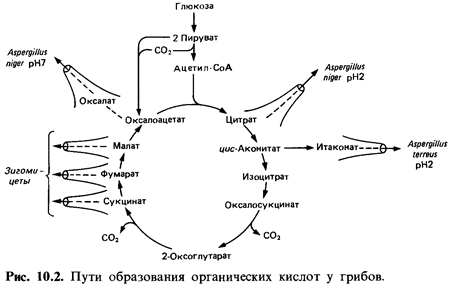
Щавелевая
кислота образуется в результате гидролиза щавелевоуксусной кислоты
под действием оксалоацетатгидролазы:
Предшественником итаконовой
кислоты служит цис-аконитовая кислота. Во время декарбоксилирования
происходит перемещение электро нов в углеродном скелете, и при этом двойная
связь переходит из положения 2,3 в положение 3,4:
Цикл
трикарбоновых кислот выполняет в первую очередь катаболи-ческую функцию. Однако
наряду с этим он служит центральным «рас пределителем», поставляющим
предшественники для синтеза многих клеточных компонентов. Если на каком-либо
участке промежуточные продукты удаляются из цикла, то на долю других реакций
выпадает за дача обеспечить цикл оксалоацетатом (щавелевоуксусной кислотой). Мы
уже упоминали
две анаплеротические реакции: 1) превращение изоцитрата
через глиоксилат и ацетил-СоА в малат и сукцинат и 2) карбоксилирование
пирувата с образованием оксало-ацетата. Из этих двух реакций более важна
вторая. Глиоксилатный цикл нужен в первую очередь для использования ацетата,
высших жирных кислот и углеводов, а также других субстратов, при распаде
которых в качестве промежуточного продукта образуется ацетил-СоА. Глюкоза часто
подавляет синтез ключевых ферментов глиоксилатного цикла (изоцитратлиазы и
малатсинтазы).
Если бы лимонная
кислота синтезировалась только из ацетил-СоА, то 1 моль глюкозы давал
бы лишь 2/3моля кислоты; это означает, что из 100 г глюкозы могло бы
образоваться только 71,1 г
лимонной кис лоты. Между тем ее выход иногда достигает 75-87 г. Исследования по казали,
однако, что происходит фиксация больших количеств С02. В опытах с14С02 метка
обнаруживалась в 6-м углеродном атоме ли монной кислоты. |