Транспорт
водорода и транспорт электронов - процессы эквивалентные. Дыхательная цепь
может рассматриваться как цепь переноса электронов. Компоненты дыхательной цепи
переходят попеременно из окисленного состояния в восстановленное и обратно, т.
е. ведут себя как типичные окислительно-восстановительные катализаторы. Они
обладают окислительно-восстановительным потенциалом, который может быть измерен
непосредствен но (у цитохромов) или косвенно (у NAD, FAD).
Окислительно-восстановительный
потенциал служит количественной мерой способности тех или иных соединений или
элементов отдавать электроны. Этот потенциал отсчитывается относительно
потенциала молекулярного водорода. Согласно определению, водородный полуэлемент
- платинированный или платиновый электрод, погруженный в раствор кислоты и
обтекаемый газообразным Н2 при давлении 1,013 бар и рН 0, имеет
потенциал, равный нулю:
Н2^;2Н++2е"
(pH0;p =1,D136ap)
Подобно
химическим элементам, биологические вещества также можно расположить в ряд по
величине их окислительно-восстановительного потенциала при степени
восстановления 1/2 (равные концентрации окисленной и восстановленной форм); эту
величину обозначают Е0. В биохимии пользуются
величиной Е„,приведенной к рН 7. При этом рН водородный электрод
имеет потенциал £„', равный - 0,42 В. На рис. 7.10 показана зависимость
потенциала, отнесенного к потенциалу водородного полуэлемента, от величины рН.
Из уравнения Нернста следует, что зависимость измеряемого потенциала
окислительно-восстановительной системы Е' от концентраций
окисленной и восстановленной форм выражается формулой
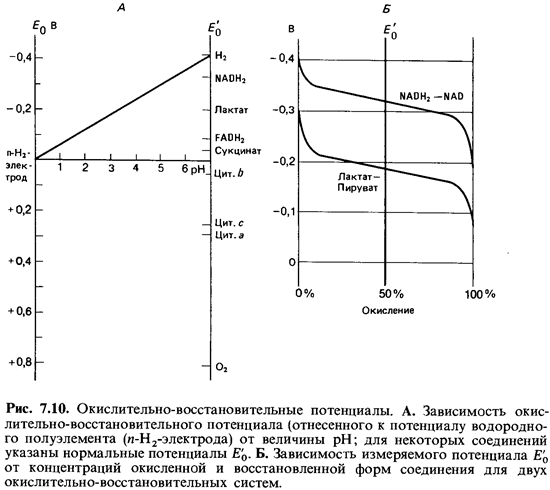
Значение Е' тем
более отрицательно, чем меньше отношение концентрации окисленной формы к
концентрации восстановленной формы (рис. 7.10, Б).
Окислительно-восстановительный
потенциал служит мерой максимальной полезной работы, которую может выполнить
система, т.е. мерой изменения свободной энергии (AG0) в
данной реакции. По разности окислительно-восстановительных потенциалов двух
реагирующих друг с другом систем Д£0 можно вычислить изменение
свободной энергии при данной реакции:
AG0 = -n-F- Д£0 =
- п 96,5 • Д£0 (кДж/моль)
Значения £0'
отдельных компонентов дыхательной цепи лежат в пределах от - 0,32 В для NADH2/NAD
[ - 0,08 В для флавопротеина (FADH2/FAD); - 0,04 В для цитохрома Ъ (Fe2 + /Fe3 +)]
до + 0,81 В для О2 ~ /'/гОг- Можно также привести значения £„'
для ряда субстратов: лактат/пируват - 0,186 В; малат/оксалоацетат - 0,166 В;
сукцинат/фурамат - 0,03 В. 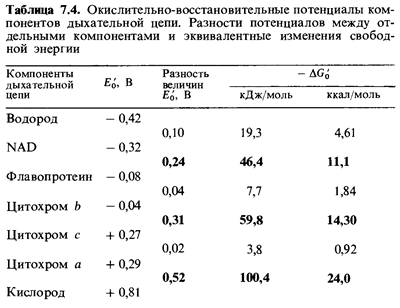
Поскольку
разность между величинами Е для Н2 и 02 составляет
- 0,42-0,81 = - 1,23 В, изменение свободной энергии в реакции гремучего газа AG0'
должно быть равно - 2-96,5-1,23 = - 237,4 кДж/моль. В клетке при переносе
водорода от NADH2 разность потенциалов составляет только [( +
0,81 В) - ( - 0,32 В)] = 1,13 В, т. е. AG0 = = - 218 кДж/моль.
Аналогичным образом по разности потенциалов можно вычислить соответствующий
выход энергии для любых двух переносчиков электронов в дыхательной цепи (табл.
7.4).
| 






